曾几何时,"每天靠创新药赚1个亿"对国内药企而言还只是遥不可及的梦想。而如今,这已成为现实。2025年上半年,中国创新药市场交出了一份令人振奋的成绩单--多家药企创新药收入大幅攀升,头部企业更是强者恒强。从百济神州的全球爆款,到恒瑞医药的转型里程碑,再到中生制药的收购布局,创新药正成为驱动药企增长的核心引擎。
一、百济一骑绝尘,双产品驱动全球竞争力
在2025年上半年国内创新药企业的激烈角逐中,百济神州以175亿元的总收入独占鳌头,稳居榜首之位。这一成绩的取得,离不开其两款核心产品--百悦泽(泽布替尼)和百泽安(替雷利珠单抗)的卓越表现。
百悦泽作为全球"Best-in-Class"产品,展现出了强大的市场竞争力,上半年销售额高达125亿元。其在国际市场上成绩斐然,已在全球75个市场获批。在美国,2025年上半年销售额总计89.58亿元,同比增长51.7%,强劲的需求增长以及净定价带来的适度利好,推动其在所有适应症领域持续拓展;在欧洲,销售额总计19.18亿元,同比增长81.4%,在德国、意大利、西班牙、法国和英国等主要市场,市场份额不断提升。百悦泽能取得如此成绩,得益于其独特的分子结构和作用机制,在与同类产品的竞争中,展现出更好的疗效和安全性,为患者提供了更优的治疗选择。
百泽安(替雷利珠单抗)同样表现出色,2025年上半年销售额总计26.43亿元,同比增长20.6%。目前已在全球47个市场获批,其销售额的增长主要得益于在中国获批新适应症纳入医保所带来的新增患者需求以及药品进院数量的增加。在国内市场,百泽安凭借其在多种肿瘤类型中的良好表现,迅速占据了一定的市场份额,为百济神州的收入增长贡献了重要力量。
百济神州的成功,是其多年来在研发领域持续投入和创新的结果。公司构建了全球化的研发、生产和商业化体系,拥有一支专业且富有创新精神的科研团队,从药物的早期研发、临床试验到生产上市,每一个环节都严格把控。通过自主研发和国际合作相结合的方式,不断推进产品的国际化进程,使得百悦泽和百泽安能够在全球多个市场获批上市并实现销售增长。这不仅为公司带来了丰厚的收入,更标志着中国创新药在全球市场上已具备强大的竞争力,能够与国际知名药企的产品一较高下,改变了全球创新药市场的竞争格局,让世界看到了中国创新药的实力。
二、恒瑞转型成功,创新药收入首超50%
在国内创新药市场的激烈竞争中,恒瑞医药也实现了重大突破,展现出强大的创新实力和转型决心。2025年上半年,恒瑞医药取得了令人瞩目的成绩,创新药收入达到75亿元,加上BD首付款合计95.6亿元。更为关键的是,其创新药收入占比首次突破50%,达到60.66%,这一里程碑事件标志着恒瑞医药已成功从传统仿制药企转型为创新驱动型企业。
恒瑞医药多年来持续加大研发投入,为创新药的研发提供了坚实的保障。2025年上半年研发投入38.71亿元,截至6月末累计研发投入近500亿元。在高研发投入的驱动下,公司创新成果不断涌现。报告期内有6款1类创新药获批上市,涵盖肿瘤、代谢、免疫等多个疾病领域,另有6项新适应症获批。目前,有100多个自主创新产品处于临床开发阶段,超过400项临床试验在全球推进。
在肿瘤领域,恒瑞的瑞维鲁胺、达尔西利等产品凭借扎实的临床数据与医保支持,保持快速放量增长。瑞维鲁胺作为一种新型雄激素受体抑制剂,在前列腺癌治疗中展现出良好的疗效和安全性,为患者提供了新的治疗选择;达尔西利作为国内首个自主研发的新型高选择性CDK4/6抑制剂,在乳腺癌治疗中也取得了显著成效,提高了患者的无进展生存期和总生存期。
在代谢领域,恒格列净等产品通过医保放量实现快速增长。恒格列净是一种新型的钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂,可通过抑制肾脏对葡萄糖的重吸收,增加尿糖排泄,从而降低血糖水平。其在2型糖尿病治疗中表现出良好的降糖效果,同时还具有减轻体重、降低血压等额外益处。
在神经科学、自免领域,新获批的富马酸泰吉利定(镇痛药)、夫那奇珠单抗(IL-17A单抗)等产品填 补国内空白,并进入医保目录。富马酸泰吉利定是一种偏向性μ阿片受体激动剂,用于治疗术后中重度疼痛,具有独特的作用机制和良好的镇痛效果;夫那奇珠单抗是一种重组抗IL-17A人源化单克隆抗体,用于治疗常规治疗疗效欠佳的活动性强直性脊柱炎成人患者,为患者带来了新的治疗希望。
恒瑞医药与默沙东、IDEAYA等企业的合作,也充分显示出其强大的对外授权能力。2025年3月,恒瑞与默沙东就Lp(a)口服小分子药物HRS-5346达成全球授权协议,获得2亿美元首付款及最高17.7亿美元的里程碑金额;4月,将SHR7280部分权益授予德国默克,获1500万欧元首付款;7月,与GSK达成合作,双方将共同开发至多12款创新药物,GSK支付5亿美元首付款,潜在交易总额约120亿美元。这些合作不仅为恒瑞带来了可观的收入,更表明其研发实力得到了国际医药巨头的认可,有助于恒瑞进一步拓展国际市场,提升全球竞争力。
三、中生、翰森、信达紧追,增速与布局并重
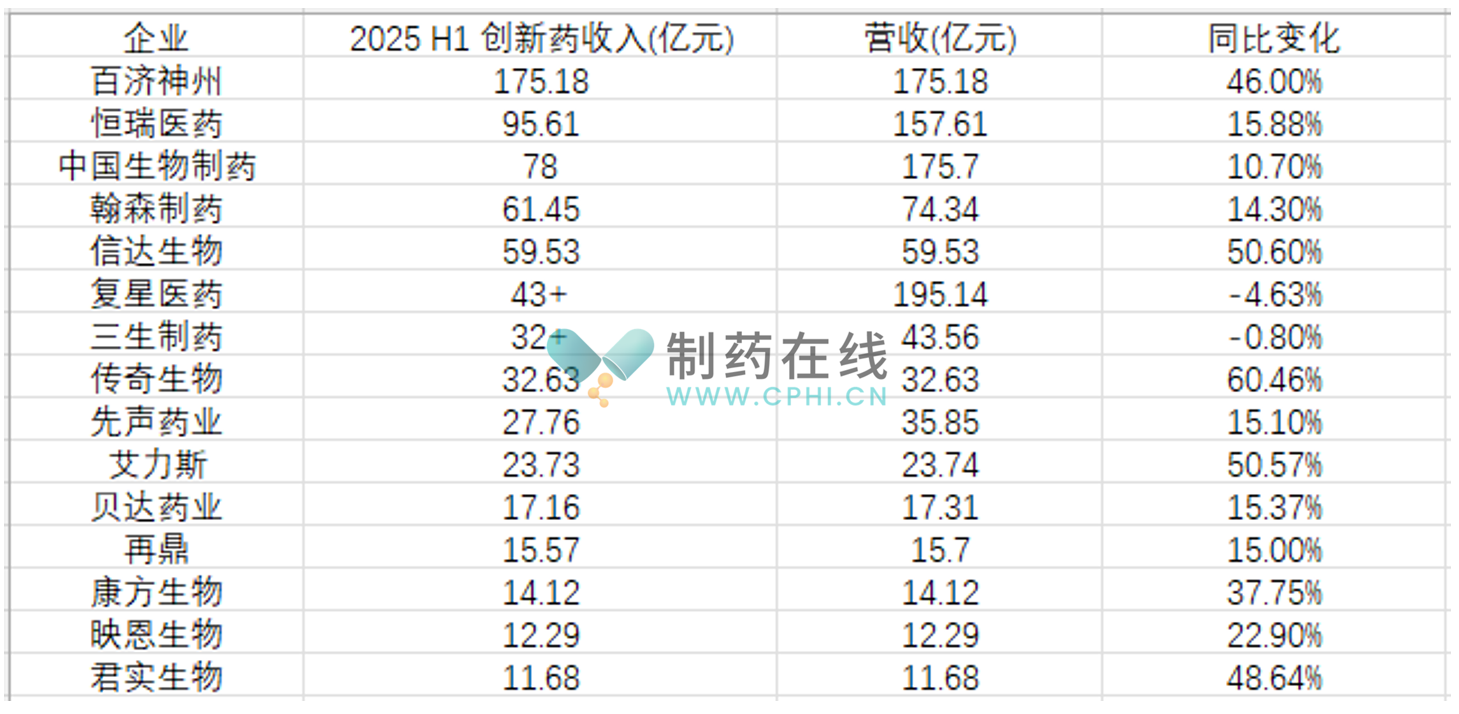
在2025年上半年国内创新药收入TOP15榜单中,中国生物制药、翰森制药、信达生物紧随百济神州和恒瑞医药之后,展现出强劲的发展态势。
中国生物制药上半年创新药收入达到78亿元,同比增长28%,在创新药收入排行榜中位列第三。公司创新产品收入占总收入比例已达44.4%,为实现"全年创新收入过半"目标奠定了关键基石。这一成绩的取得,得益于公司多年来在创新研发上的持续投入和战略布局。2025年上半年,公司研发费用投入达31.9亿元,较上年同期增加6.1亿元,研发费用占收入比例达到18.1%,其中创新药及生物类似药研发费用占比达到78%。过去两年,公司获批创新产品高达11个,已进入密集收获期。2025年以来,多个创新产品获批,包括国内首 款24小时长效镇痛非甾体抗炎药(NSAID)注射液普坦宁、首个国产重组七因子安启新等;"国药之光"安罗替尼新获批一线肾细胞癌、一线软组织肉瘤两个适应症,适应症总数已达到9个;HER2ADC双抗TQB2102、CCR8单克隆抗体LM-108、JAK/ROCK抑制剂罗伐昔替尼片被纳入突破性治疗品种,有望加速审批。
在研发布局上,中国生物制药在肿瘤、肝病、呼吸、外科/镇痛四大重点治疗领域均有突出进展,多项全球FIC/BIC产品研发进度喜人。在肿瘤领域,全面布局非小细胞肺癌领域,覆盖多种分型的全线治疗,EGFR/cMet双抗TQB2922即将启动二线非小细胞肺癌III期临床,EGFR/cMet双抗ADCTQB6411I期临床正在入组,两款产品进度均位于中国前列;深度布局乳腺癌三大亚型,CDK2/4/6抑制剂库莫西利胶囊有望成为HR+/HER2-乳腺癌的BIC疗法,HER2双抗ADCTQB2102较DS-8201潜在安全性优效,多个适应症正在同步拓展,其中三项乳腺癌III期快速推进;系统布局消化道领域结直肠癌、胃癌、胰腺癌、肝癌等核心癌肿,LM-108(CCR8单抗)、TQB2868(PD-1/TGF-β双功能融合蛋白)研发进度全球最快,且目前临床数据展示出了极大潜力。2025年7月,公司以5亿美元的净对价全资收购上海创新药企礼新医药,进一步强化了在肿瘤创新领域的核心竞争力与国际影响力。礼新医药拥有自主研发的抗体、ADC、TCE及肿瘤微环境四大技术平台,其双抗和ADC平台已获国际巨头认可,此次收购将有助于中国生物制药加速创新资产转化,完善在肿瘤领域的创新布局。
翰森制药上半年创新药与合作产品销售收入约61.45亿元,同比增长22.1%,占公司总收入比例约82.7%,已成为驱动公司业绩可持续增长的核心动力,在创新药收入排行榜中位列第四。公司上半年实现收入74.34亿元,同比增长14.3%;净利润31.35亿元,同比增长15%。翰森制药在中国产生销售收入的创新药共七款,从疾病领域来看,抗肿瘤板块上半年贡献收入最多,达到约45.31亿元,占总收入的比重约60.9%,包括中国首个原研三代EGFR-TKI抑制剂甲磺酸阿美替尼片、中国首个原研慢性髓性白血病新型二代TKI创新药甲磺酸氟马替尼片等。6月4日,甲磺酸阿美替尼片获英国药品与保健品监管局(MHRA)批准上市,成为公司首个获准进入海外市场的创新药,同时也是首个海外上市的中国原研EGFR-TKI,标志着翰森制药在国际化进程中迈出了重要一步。
代谢及其他疾病板块上半年收入约14亿元,占总收入的比重约18.8%,核心产品聚乙二醇洛塞那肽注射液是国产首 款原研GLP-1受体激动剂周制剂、全球第一款PEG化的GLP-1周制剂,2019年5月获批用于二型糖尿病,2020年通过医保谈判首次被纳入国家医保目录,并于2024年11月成功续约纳入,降血糖疗效明确,兼有减重、降脂、降压以及肾脏和心血管获益。在BD合作方面,翰森制药成果丰硕。2025年6月,授予Regeneron(再生元公司)GLP-1/GIP双受体激动剂HS-20094海外独占许可,潜在最高总金额超20亿美元,相关临床研究已累计给药超一千名受试者,目前HS20094正在积极推进用于肥胖或超重的三期临床研究,公司已于2025年7月获得8000万美元首付款。2024年12月与默沙东签署关于HS-10535的全球独家许可协议,此次合作潜在最高总金额超过20亿美元,2025年上半年自默沙东收取的BD许可费首付款计入合作收入1.12亿美元。2023年10月与葛兰素史克(GSK)就ADC肿瘤新药HS-20089达成独家许可协议,收取8500万美元首付款,并有资格收取最多14.85亿美元里程碑付款;2023年12月又与GSK就另一款ADC新药HS-20093达成独家许可协议,获得1.85亿美元首付款,并有资格获得最多15.25亿美元的成功里程碑付款,HS-20093已获美国食品药品监督管理局(FDA)突破性疗法认定(BTD),在国内也有三个适应证被纳入突破性治疗药物,用于小细胞肺癌适应证的治疗已进入三期临床研究阶段。
信达生物上半年实现营业收入59.53亿元,同比增长50.6%,在创新药收入排行榜中位列第五。录得净利润(Non-IFRS)12.13亿元,上年同期为亏损1.6亿元,实现了扭亏为盈。收入增长主要得益于肿瘤产品的强劲表现、综合产品线扩展及授权费收入增加。其中,产品销售收入为52.34亿元,同比增长37.3%,贡献核心收入增量;授权费收入达6.66亿元,较去年同期的1.16亿元显著增长,主要来自与罗氏签订独家许可及合作协议所收取的首付款。信达生物目前已有16款新药获批上市(6款已纳入国家医保乙类目录),包括13款创新药及3款生物类似药,形成了以抗肿瘤为核心,代谢、自免、眼科三大领域为补充的丰富产品线。
在抗肿瘤领域,拳头产品达伯舒(信迪利单抗)是国内获批的第2款国产PD-1单抗,自2018年上市至今已累计拓展8个适应症(含附条件批准),其中有7个已被纳入国家医保,随着适应症的不断扩大,叠加医保的积极作用,该药近年来在中国三大终端六大市场的销售额保持以两位数的增速增长,2024年其销售额超过40亿元,2025年一季度超过15亿元,其中院内市场(公立医院+公立基层医疗)销售占比超过90%。达攸同(贝伐珠单抗)是信达生物获批的首 款生物类似药,已成长为公司第二大支柱产品,近年来在中国三大终端六大市场的销售额持续增长,且增速呈逐年递增态势,2024年其销售额突破20亿元,2025年一季度超过6亿元。在非肿瘤领域,信必乐(托莱西单抗)为国内首个本土原研的PCSK9抑制剂,2024年12月纳入国家医保目录,2025年一季度在中国三大终端六大市场的销售额增速超过900%;信尔美(玛仕度肽)于2025年6月获批,为全球首个GLP-1R/GCGR双靶点激动剂,分析师预测其销售峰值有望突破80亿元,虽然上市销售的时间比较短,但市场反馈"非常不错",公司重点放在品牌构建以及全渠道布局上,目前的渠道除了覆盖传统的公立医院、民营医院体系外,正在积极拓展电商平台以及零售药店终端,京东健康数据显示,7月4日至8月4日,"信尔美"关键词在京东平台的搜索量已突破百万,首发当月已累计服务用户数超3万。
信达生物还有52款新药(不含已获批/撤回品种)在国内处于申请临床及以上阶段,包括47款大分子生物药及5款小分子化学药,新药管线覆盖了肿瘤、自身免疫、眼科、消化代谢等多个疾病领域。在抗肿瘤领域,4款新药处于III期临床及以上阶段,其中伊匹木单抗于2025年2月提交NDA在审,有望成为国内首个伊匹木单抗生物类似药,原研产品2024年全球销售额超过25亿美元;IBI126、IBI354、IBI343三款ADC处于III期临床,分别靶向CEACAM5、HER2及Claudin18.2,目前全球暂无靶向CEACAM5、Claudin18.2的ADC获批,信达生物均处于研发第一梯队。此外,20余款抗肿瘤1类新药处于I期或II期临床,涉及多个IO(免疫肿瘤)疗法及ADC,如PD-1/IL-2a偏向双特异性抗体融合蛋白IBI363步入II期临床,有望为冷肿瘤和免疫耐药患者提供新的用药选择;三特异性T细胞连接器IBI3003(BCMA/GPRC5D/CD3)处于I/II期临床,具备超越CAR-T和双抗的潜力。在新一代ADC方面,前瞻性布局了双抗ADC和双载荷ADC,包括IBI3014(TROP2/PD-L1双抗ADC)、IBI3020(CEACAM5双载荷ADC)、IBI3005(EGFR/HER3双抗ADC)等。
四、大单品突围,传奇、艾力斯靠"一招鲜"闯天下
在2025年上半年国内创新药收入TOP15榜单中,除了那些通过全线布局取得优异成绩的企业外,还有传奇生物和艾力斯两家药企凭借单一爆款产品成功跻身榜单,展现出在细分领域深耕的独特优势。
传奇生物依靠西达基奥仑赛(CAR-T产品)在2025年上半年取得了亮眼的成绩。西达基奥仑赛是一种靶向B细胞成熟抗原(BCMA)的嵌合抗原受体T细胞(CAR-T)疗法,2022年2月获得美国FDA批准上市,用于治疗复发或难治性多发性骨髓瘤成人患者的末线治疗。此后,又陆续在欧盟、日本、中国等多个国家和地区上市。2025年上半年,西达基奥仑赛销售收入达到58亿元(8.08亿美元),传奇生物分得30亿元。其中,在2025年第一季度,强生披露Carvykti(西达基奥仑赛)销售额为3.69亿美元,约合26.5亿元,同比增长135%,美国市场收入3.18亿美元,同比增长127%。西达基奥仑赛能取得如此高的销售额,得益于其显著的疗效和良好的安全性。在临床试验中,该产品展现出了高缓解率,为复发或难治性多发性骨髓瘤患者提供了有效的治疗选择,满足了这一细分领域未被满足的临床需求。同时,传奇生物与强生的合作,借助强生强大的全球商业化能力,使得西达基奥仑赛能够快速进入全球多个市场,实现销售额的快速增长。
艾力斯则凭借伏美替尼这一单产品在创新药市场中占据了一席之地。伏美替尼是一种第三代EGFR-TKI抑制剂,2021年3月在国内获批上市,主要用于EGFR敏感突变、EGFRT790M耐药突变的晚期非小细胞肺癌治疗。自上市以来,伏美替尼销售额增长迅速,2025年上半年实现销售收入23.6亿元,同比增长51.76%,成为推动艾力斯业绩增长的核心产品。2021-2024年其销售收入分别为2.36亿元、7.90亿元、19.78亿元、35.06亿元,2022-2024年的同比增速分别为235.29%、150.22%、77.27%。伏美替尼的成功,源于其在疗效和安全性方面的优势。在临床研究中,伏美替尼显示出了良好的抗肿瘤活性,能够有效延长患者的无进展生存期。同时,其安全性良好,不良反应可控,提高了患者的生活质量。此外,艾力斯不断推进伏美替尼的新适应症拓展,包括20外显子插入突变一线及二线治疗适应症、PACC突变的一线治疗适应症、针对EGFR敏感突变阳性的非鳞NSCLC伴脑转移患者的治疗、EGFR非经典突变非小细胞肺癌的辅助治疗等均处于注册临床阶段。其中,伏美替尼拟用于二线治疗EGFR20外显子插入突变的局部晚期或转移性NSCLC成人患者的NDA在2025年7月被CDE受理并纳入拟优先审评品种,有望明年获批上市;公司与ArriVent合作开发的伏美替尼适用于20外显子插入突变NSCLC一线治疗的全球、多中心、III期临床研究已于2025年一季度完成患者入组工作。新适应症的拓展将进一步扩大伏美替尼的市场空间,为艾力斯带来持续的业绩增长动力。
传奇生物和艾力斯的成功表明,在创新药市场中,即使企业没有全面的产品线布局,只要能够在细分领域做到极 致,打造出具有核心竞争力的爆款产品,同样可以在激烈的市场竞争中占据一席之地。专注于细分领域,深入挖掘未被满足的临床需求,通过持续的研发创新和临床研究,不断优化产品的疗效和安全性,结合有效的商业化策略,将产品推向市场并获得认可,是这些企业取得成功的关键。这也为其他创新药企提供了一种可行的发展思路,鼓励企业在资源有限的情况下,聚焦优势领域,集中力量打造拳头产品,实现差异化发展。
结语
从TOP15榜单不难看出,中国创新药市场正进入收获期。头部企业凭借多产品布局和国际化能力持续领先,中型企业则通过差异化产品和BD合作快速跟进。创新药已不再只是"未来故事",而是实打实的业绩支撑。随着更多产品进入医保、走向全球,中国药企的创新成果还将进一步释放。未来,能否持续研发出具有临床价值的药物、能否高效推进商业化落地,将成为药企能否守住排名的关键。中国创新药,正在迎来属于自己的黄金时代。
参考来源:Insight数据库;公开资料整理